Химические свойства алкенов получение вариант 1. Физические свойства алкенов, применение, способы получения
Алкены — это непредельные углеводороды , которые имеют одну двойную связь между атомами . Другое их название это олефины, оно связано с историей открытия этого класса соединений. В основном в природе эти вещества не встречаются, а синтезируются человеком для практических целей. В номенклатуре ИЮПАК название этих соединений формируется по тому же принципу, что и для алканов, только суффикс “ан” заменяется на “ен”.
Вконтакте
Строение алкенов
Два атома углерода, участвующих в образовании двойной связи, всегда находятся в sp2 гибридизации, и угол между ними равен 120 градусам. Двойная связь образована с помощью перекрывания π -π орбиталей, а оно не очень прочное, поэтому данную связь достаточно просто разорвать, что находит применение в химических свойствах веществ.
Изомерия
По сравнению с предельными, в этих углеводородах возможно больше видов , при том как пространственной, так и структурной. Структурная изомерия может также подразделяться на несколько видов.
Первый также существует и для алканов, и заключается в различном порядке соединения атомов углерода. Так изомерами могут быть пентен-2 и 2-метилбутен-2. А второй — это изменение положения двойной связи.
Пространственная изомерия в этих соединениях возможна благодаря появлению двойной связи. Она бывает двух видов — геометрической и оптической.
Геометрическая изомерия — один из самых распространенных в природе видов, при том практически всегда геометрические изомеры будут иметь кардинально разные физические и химические свойства. Различают цис и транс изомеры. У первых — заместители располагаются с одной стороны от кратной связи, а у транс изомеров они находятся в разных плоскостях.
Получение алкенов
 Впервые получены они были, как и много других веществ, совершенно случайно.
Впервые получены они были, как и много других веществ, совершенно случайно.
Немецкий химик и исследователь Бехер в конце 17 века изучал действие серной кислоты на этиловый спирт и понял, что получил неизвестный газ , который при этом является более реакционноспособным, чем метан.
Позже подобные исследования провели еще несколько ученых, они же и узнали, что данный газ при взаимодействии с хлором образует маслянистое вещество.
Поэтому первоначально этому классу соединений было присвоено название олефины, что переводится как маслородный. Но все же определить состав и строение данного соединения у ученых не получалось. Это произошло только почти спустя два века, в конце девятнадцатого столетия.
В настоящее время существует много способов получения алкенов.
Промышленные способы
Получение промышленными методами :
- Дегидрирование предельных углеводородов. Данная реакция возможна только при действии высоких температур (около 400 градусов) и катализаторов — либо оксида хрома 3, либо алюмоплатиновых катализаторов.
- Дегалогенирование дигалогеноалканов. Происходит только в присутствии цинка или магния, и при высоких температурах.
- Дегидрогалогенирование галогеноалканов. Проводится при помощи натриевых или калиевых солей органических кислот при повышенной температуре.
Важно ! Данные способы получения алкенов не дают чистого продукта, результатом реакции будет смесь непредельных углеводородов. Преобладающее среди них соединение определяется с помощью правила Зайцева. Оно гласит, что водород отщепляется с наибольшей вероятностью от атома углерода у которого меньше всего связей с водородами.
Дегидратация спиртов. Может проводиться только при нагревании и в присутствии растворов сильных минеральных кислот, обладающих водоотнимающим свойством.
Гидрирование алкинов. Возможно только в присутствии паладиевых катализаторов.
Химические свойства алкенов
Алкены являются очень химически активными веществами. Во многом это объясняется благодаря наличию двойной связи. Самыми характерными реакциями для этого класса соединений являются электрофильное и радикальное присоединение.
- Галогенирование алкенов — относится к классическим реакциям электрофильного присоединения. Она происходит только в присутствии инертных органических растворителей, чаще всего это тетрахлорметан.
- Гидрогалогенирование. Присоединение этого типа осуществляется по правилу Марковникова. Ион присоединяется к более гидрированному атому углерода возле двойной связи, и соответственно, ион галогенида присоединяется ко второму атому углерода. Это правило нарушается в присутствии перекисных соединений — эффект Харроша. Присоединение галогеноводорода происходит полностью обратно правилу Марковникова.
- Гидроборирование. Эта реакция имеет значительную практическую важность. Поэтому ученый, который ее открыл и изучил даже получил Нобелевскую премию. Данная реакция проводится в несколько ступеней, при этом присоединение иона бора происходит не по правилу Марковникова.
- Гидратация алкенов или присоединение . Данная реакция также протекает согласно правилу Марковникова. Гидроксид-ион присоединяется к наименее гидрированному атому углерода при двойной связи.
- Алкилирование — еще одна реакция часто применяемая в промышленности. Она заключается в присоединении предельных углеводородов к непредельным под воздействием низких температур и катализаторов, с целью увеличения атомной массы соединений. Катализатором чаще всего выступают сильные минеральные кислоты. Также эта реакция может протекать и по свободнорадикальному механизму.
- Полимеризация алкенов — еще одна нехарактерная для предельных углеводородов реакция. Она подразумевает соединение между собой многочисленных молекул с целью образования прочного соединения, отличающегося по своим физическим свойствам.
 n в данной реакции это количество молекул, вступивших в связь. Обязательным условием осуществления является кислая среда, повышенная температура и увеличенное давление.
n в данной реакции это количество молекул, вступивших в связь. Обязательным условием осуществления является кислая среда, повышенная температура и увеличенное давление.
Также для алкенов характерны и другие реакции электрофильного присоединения, которые не получили такого обширного практического распространения.
Например, реакция присоединения спиртов, с образованием простых эфиров.
Или присоединение хлорангидридов, с получением непредельных кетонов — реакция Кондакова.
Обратите внимание! Данная реакция возможна только в присутствии катализатора хлорида цинка.
Следующий крупный класс реакций характерный для алкенов это реакции радикального присоединения. Данные реакции возможны только при образовании свободных радикалов под воздействием высоких температур, облучения и других действий. Самая характерная реакция радикального присоединения это гидрирование с образованием предельных углеводородов. Она происходит исключительно под воздействием температур и в присутствии платинового катализатора.
Благодаря наличию двойной связи, для алкенов очень характерными являются различные реакции окисления .
- Горение — классическая реакция окисления. Она хорошо идет без катализаторов. В зависимости от количества кислорода возможны разные конечные продукты: от углекислого газа и до углерода.
- Окисление перманганатом калия в нейтральной среде. Продуктами являются многоатомные спирты и бурый осадок диоксида марганца. Данная реакция считается качественной для алкенов.
- Также мягкое окисление может осуществляться пероксидом водорода, оксидом осмия 8, и другими окислителями в нейтральной среде. Для мягкого окисления алкенов характерен разрыв только одной связи, продуктом реакции, как правило, являются многоатомные спирты.
- Также возможно и жесткое окисление, при котором происходит разрыв обеих связей и образуются кислоты или кетоны. Обязательным условием является кислая среда, чаще всего используют серную кислоту, так как другие кислоты могут также подвергаться окислению с образованием побочных продуктов.
Физические свойства алкенов
 Газами в нормальных условиях являются только этилен, пропен и бутен.
Газами в нормальных условиях являются только этилен, пропен и бутен.
Начиная с пентена, и до гептодецена, все алкены находятся в жидком состоянии.
И все остальные являются твердыми веществами.
Температуры плавления и кипения пропорционально увеличиваются с ростом молекулярной массы, но могут меняться для изомеров.
Все алкены не растворяются в воде , но хорошо растворяются в инертных органических растворителях.
Применение алкенов
Алкены довольно широко используются в промышленности и применяются для синтеза большого количества веществ. Например, при помощи этилена синтезируют поливинилхлорид(ПВХ), стирол, этиленгликоль, этанол, полиэтилен, каучуки и множество других веществ. Наибольший объем пропилена используют для получения полипропилена.
Алкены — строение, свойства, применение
Изучаем химию — свойства алкенов, применение в промышленности
Вывод
В общем, можно точно сказать, что алкены благодаря своим химическим свойствам являются очень востребованными в промышленности. Они участвуют в производстве самых разнообразных пластмасс, каучуков и множества других веществ.
Низшие алкены (С 2 - С 5), в промышленных масштабах получают из газов, образующихся при термической переработке нефти и нефтепродуктов. Алкены можно также получить, используя лабораторные методы синтеза.
4.5.1. Дегидрогалогенирование
При обработке галогеналканов основаниями в безводных растворителях, например, спиртовым раствором едкого кали, происходит отщепление галогеноводорода.
4.5.2. Дегидратация
При нагревании спиртов с серной или фосфорной кислотами происходит внутримолекулярная дегидратация ( - элиминирование).
Преобладающее направление реакции, как и в случае дегидрогалогенирования, - образование наиболее устойчивого алкена (правило Зайцева).
Дегидратацию спиртов можно провести, пропуская пары спирта над катализатором (оксиды алюминия или тория) при 300 - 350 о С.
4.5.3. Дегалогенирование вицинальных дигалогенидов
Действием цинка в спирте дибромиды, содержащие галогены у соседних атомов (вицинальные), могут быть превращены в алкены.

4.5.4. Гидрирование алкинов
При гидрировании алкинов в присутствии платинового или никелевого катализаторов, активность которых уменьшена добавлением небольшого количества соединений свинца (каталитический яд), образуется алкен, который не подвергается дальнейшему восстановлению.
4.5.5. Восстановительное сочетание альдегидов и кетонов
При обработке алюмогидридом лития и хлоридом титана(III) из двух молекул альдегида или кетона с хорошими выходами образуются ди- или соответственно тетразамещённые алкены.

5. АЛКИНЫ
Алкинами называются углеводороды, содержащие тройную углерод-углеродную связь –СС–.
Общая формула простых алкинов С n H 2n-2 . Простейшим представителем класса алкинов является ацетилен H–СС–H, поэтому алкины называют также ацетиленовыми углеводородами.
5.1. Строение ацетилена
Атомы углерода ацетилена находятся в sp -гибридном состоянии. Изобразим орбитальную конфигурацию такого атома. При гибридизации 2s -орбитали и 2р -орбитали образуются две равноценные sp -гибридные орбитали, расположенные на одной прямой, и остаются две негибридизованные р -орбитали.

Рис. 5.1 Схема формирования sp -гибридных орбиталей атома углерода
Направленияи формы орбиталей s р -гибридизованного атома углерода: гибридизованные орбитали эквивалентны, максимально удалены друг от друга
В молекуле ацетилена простая связь ( - связь) между атомами углерода образована перекрыванием двух sp -гибридизованных орбиталей. Две взаимно перпендикулярные - связи возникают при боковом перекрывании двух пар негибридизованных 2р- орбиталей, - электронные облака охватывают скелет так, что электронное облако имеет симметрию, близкую к цилиндрической. Связи с атомами водорода образуются за счёт sp -гибридных орбиталей атома углерода и 1s -орбитали атома водорода, молекула ацетилена линейна.

Рис. 5.2 Молекула ацетилена
а - боковое перекрывание 2р орбиталей дает две -связи;
б - молекула линейна, -облако имеет цилиндрическую форму
В пропине простая связь ( - связь) С sp -С sp3 короче аналогичной связи С sp -С sp2 в алкенах, это объясняется тем, что sp- орбиталь ближе к ядру, чем sp 2 - орбиталь .
Тройная углерод-углеродная связь С С короче двойной связи, а общая энергия тройной связи приблизительно равна сумме энергий одной простой связи С–С (347 кДж/моль) и двух -связей (259·2 кДж/моль) (табл. 5.1).
Самыми простыми органическими соединениями являются предельные и непредельные углеводороды. К ним относят вещества класса алканов, алкинов, алкенов.
Формулы их включают атомы водорода и углерода в определенной последовательности и количестве. Они часто встречаются в природе.
Определение алкенов
Другое их название - олефины или углеводороды этиленовые. Именно так назвали данный класс соединений в 18 столетии при открытии маслянистой жидкости − хлористого этилена.
К алкенам относятся вещества, состоящие из водородных и углеродных элементов. Они относятся к ациклическим углеводородам. В их молекуле присутствует единственная двойная (ненасыщенная) связь, соединяющая два углеродных атома между собой.
Формулы алкенов
Каждый класс соединений имеет свое химическое обозначение. В них символами элементов периодической системы указывается состав и структура связи каждого вещества.

Общая формула алкенов обозначается следующим образом: C n H 2n , где число n больше или равняется 2. При ее расшифровке видно, что на каждый атом углерода приходится по два атома водорода.
Молекулярные формулы алкенов из гомологического ряда представлены следующими структурами: C 2 H 4 , C 3 H 6 , C 4 H 8 , C 5 H 10 , C 6 H 12 , C 7 H 14 , C 8 H 16 , C 9 H 18 , C 10 H 20 . Видно, что каждый последующий углеводород содержит на один больше углерода и на 2 больше водорода.
Существует графическое обозначение расположения и порядка химических соединений между атомами в молекуле, которое показывает формула алкенов структурная.С помощью валентных черточек обозначается связь углеродов с водородами.
Формула алкенов структурная может быть изображена в развернутом виде, когда показываются все химические элементы и связи. При более кратком выражении олефинов не показывается соединение углерода и водорода с помощью валентных черточек.
Формулой скелетной обозначают самую простую структуру. Ломаной линией изображают основу молекулы, в которой атомы углерода представлены ее верхушками и концами, а звеньями указывают водород.
Как образуются наименования олефинов
CH 3 -HC=CH 2 + H 2 O → CH 3 -OHCH-CH 3 .
При воздействии на алкены кислотой серной происходит процесс сульфирования:
CH 3 -HC=CH 2 + HO−OSO−OH → CH 3 -CH 3 CH-O−SO 2 −OH.
Реакция протекает с образованием кислых эфиров, например, изопропилсерной кислоты.
Алкены подвержены окислению во время их сжигания при действии кислорода с формированием воды и газа углекислого:
2CH 3 -HC=CH 2 + 9O 2 → 6CO 2 + 6H 2 O.
Взаимодействие олефиновых соединений и разбавленного калия перманганата в форме раствора приводит к возникновению гликолей или спиртов двухатомного строения. Данная реакция также является окислительной с образованием этиленгликоля и обесцвечиванием раствора:
3H 2 C=CH 2 + 4H 2 O+ 2KMnO 4 → 3OHCH-CHOH+ 2MnO 2 +2KOH.
Молекулы алкенов могут быть задействованы в процессе полимеризации со свободнорадикальным или катионно-анионным механизмом. В первом случае под влиянием пероксидов получается полимер типа полиэтилена.
По второму механизму катионными катализаторами выступают кислоты, а анионными являются вещества металлорганические с выделением стереоселективного полимера.
Что такое алканы
Их еще называют парафинами или предельными ациклическими углеводородами. Они обладают линейной или разветвлённой структурой, в которой содержатся только насыщенные простые связи. Все представители данного класса имеют общую формулу C n H 2n+2 .

В их составе присутствуют только атомы углерода и водорода. Общая формула алкенов образуется из обозначения предельных углеводородов.
Названия алканов и их характеристика
Самым простым представителем данного класса является метан. За ним следуют вещества типа этана, пропана и бутана. В основе их названия лежит корень числительного на греческом языке, к которому прибавляют суффикс -ан. Наименования алканов занесены в IUPAC номенклатуру.
Общая формула алкенов, алкинов, алканов включает только две разновидности атомов. К ним относятся элементы углерода и водорода. Количество углеродных атомов во всех трех классах совпадает, отличие наблюдается только в численности водорода, который может отщепляться или присоединяться. Из получают ненасыщенные соединения. У представителей парафинов в молекуле содержится на 2 атома водорода больше, чем у олефинов, что подтверждает общая формула алканов, алкенов. Алкенов структура считается ненасыщенной за счет наличия двойной связи.
Если соотнести число во-до-ро-дных и уг-ле-ро-дных ато-мов в ал-ка-нах, то значение будет мак-си-маль-ным в сравнении с другими классами уг-ле-во-до-ро-дов.
Начиная с метана и заканчивая бутаном (от С 1 до С 4), вещества существуют в газообразном виде.
В жидкой форме представлены углеводороды гомологического промежутка от С 5 до С 16 . Начиная с алкана, имеющего в основной цепи 17 атомов углерода, происходит переход физического состояния в твердую форму.
Для них характерна изомерия по углеродному скелету и оптические видоизменения молекулы.

В парафинах углеродные ва-лент-но-сти считаются полностью за-ня-тыми соседними уг-ле-ро-да-ми или во-до-ро-да-ми с образованием связи σ-типа. С хи-ми-че-ской точки зрения это обуславливает их слабые свой-ства, именно поэтому алканы носят название пре-дель-ны-х или на-сы-щен-ны-х уг-ле-во-до-ро-дов, лишенных сродства.
Они вступают в реакции замещения, связанные с галогенированием по радикальному типу, сульфохлорированием или нитрованием молекулы.
Парафины подвергаются процессу окисления, горения или разложения при высоких температурах. Под действием ускорителей реакций происходит отщепление атомов водорода или дегидрирование алканов.
Что такое алкины
Их еще называют ацетиленовыми углеводородами, у которых в цепочке углеродной присутствует тройная связь. Структура алкинов описывается общей формулой C n H 2 n-2 . Из нее видно, что в отличие от алканов, у ацетиленовых углеводородов недостает четыре атома водорода. Их заменяет тройная связь, образованная двумя π- соединениями.
Такое строение обуславливает химические свойства данного класса. Структурная формула алкенов и алкинов наглядно показывает ненасыщенность их молекул, а также наличие двойной (H 2 C꞊CH 2) и тройной (HC≡CH) связи.
Наименование алкинов и их характеристика
Самым простым представителем является ацетилен или HC≡CH. Его также именуют этином. Происходит оно от названия насыщенного углеводорода, в котором убирают суффикс -ан и добавляют -ин. В наименованиях длинных алкинов цифрой указывают расположение тройной связи.
Зная строение углеводородов насыщенных и ненасыщенных, можно определить, под какой буквой обозначена общая формула алкинов: а) CnH2n; в) CnH2n+2; c) CnH2n-2; г) CnH2n-6. Правильным ответом будет третий вариант.
Начиная с ацетилена и заканчивая бутаном (от С 2 до С 4), вещества имеют газообразную природу.

В жидкой форме находятся углеводороды гомологического промежутка от С 5 до С 17 . Начиная с алкина, имеющего в основной цепи 18 атомов углерода, происходит переход физического состояния в твердую форму.
Для них характерна изомерия по углеродному скелету, по положению связи тройной, а также межклассовые видоизменения молекулы.
По химическим характеристикам ацетиленовые углеводороды подобны алкенам.
Если у алкинов тройная связь концевая, то они выполняют функцию кислоты с образованием солей алкинидов, например, NaC≡CNa. Наличие двух π-связей делает молекулу ацетиледина натрия сильным нуклеофилом, вступающим в реакции замещения.
Ацетилен подвергается хлорированию в присутствии хлорида меди с получением дихлорацетилена, конденсации под действием галогеналкинов с выделением диацетиленовых молекул.
Алкины участвуют в реакциях принцип которых лежит в основе галогенирования, гидрогалогенирования, гидротации и карбонилирования. Однако такие процессы протекают слабее, чем у алкенов с двойной связью.
Для ацетиленовых углеводородов возможны реакции присоединения по нуклеофильному типу молекулы спирта, первичного амина или сероводорода.
4.3.б. Присоединение галогеноводородов (гидрогалогенирование)
Другой важной реакций электрофильного присоединения к алкенам является давно известное гадрогалогенирование алкенов.
Ниже приведены типичные примеры присоединения HCl, HBr и HI к различным алкенам.


Влияние алкильных заместителей у двойной связи на скорость присоединения описывается следующей последовательностью:
R 2 C=CHR > RCH=CHR > RCH=CH 2
Это согласуется с таким механизмом, в котором в определяющей скорость стадии реакции происходит образование карбокатиона, поскольку стабильность алкильных катионов убывает в ряду третичный > вторичный > первичный. Таким образом, механизм присоединения должен включать промежуточное образование или свободного карбокатиона, что наблюдается редко, или интермедиата с карбокатионным характером. Последний случай наиболее типичен.
Если бы присоединение происходило через "свободный карбокатион", то реакция была бы совершенно нестереоселективной, так, как алкильные катионы имеют плоское строение. Однако, гидрогалогенирование, как правило, протекает стереоселективно, причем в зависимости от типа алкена может наблюдаться селективное анти -присоединение, селективное син - или смешанное син -анти -присоединение.
Для алкенов, у которых двойная связь не сопряжена с ароматическим кольцом, характерно анти -присоединение галогеноводорода. Анти -присоединение хлористого и бромистого водорода, хлористого и бромистого дейтерия наблюдается для циклогексена, циклопентена, 1,2-диметилгексена, 1,2-диметилпентена, цис - и транс -бутена-2, гексена-3 и многих других простых алкенов и циклоалкенов.

В продукте присоединения одинаковые заместители (метильные группы) расположены по разные стороны средней плоскости циклогексанового кольца, следовательно он относится к транс -ряду. Анти -присоединение трудно совместимо с механизмом, в котором предполагается образование дискретного карбокатиона. Для плоского карбокатиона нуклеофильная атака галогенид-иона равновероятна с обеих сторон плоскости, что должно привести к образованию смеси продуктов син - и анти -присоединения. Кинетика гидрогалогенирования алкенов также указывает на более сложный механизм присоединения. Для несопряженных алкенов скорость реакции описывается уравнением третьего порядка со вторым порядком по галогеноводороду, т. е. соответствует Ad E 3-механизму.
v = k [алкен] 2
Анти-присоединение и второй порядок реакции по галогеноводороду хорошо согласуется с Ad E 3-механизмом, в котором алкен взаимодействует с двумя молекулами галогеноводорода, одна из которых выполняет функцию электрофильного, а другая - нуклеофильного агента.

Такой тримолекулярный механизм предполагает, что первоначально образуется комплекс алкена и одной молекулой галогеноводорода с последующей атакой второй молекулы НХ на этот комплекс с анти -стороны без образования дискретного карбокатиона. Следует особо отметить, что любой тримолекулярный механизм должен состоять из двух последовательных стадий, поскольку одновременно столкновение трех молекул крайне маловероятно.

Анти-присоединение свидетельствует о предпочтительной нуклеофильной атаке галогеноводорода со стороны противоположной той, откуда происходит протонирование алкена. Вместо галогеноводорода функцию нуклеофильного агента в конечной стадии может выполнить и галогенид-ион. Действительно, скорость реакции обычно возрастает прямо пропорционально концентрации галогенид-иона, введенного в реакционную смесь в виде галогенидов тетраалкиламмония NR 4+ X - или лития LiX. В этом случае наблюдается стереоспецифическое анти -присоединение.
Для алканов, у которых двойная связь сопряжена с ароматическим кольцом, характерно син -присоединение или смешанное син -анти -присоединение галогеноводорода, например:

Син-присоединение является доминирующим процессом для цис - и транс -изомеров 1-фенилпропена, 1-фенил-4-алкилциклогексенов, аценафтилена, индена. При протонировании таких алкенов образуются карбокатионы бензильного типа, которые стабильнее чисто алкильных катионов, возникающих при протонировании обычных алкенов и циклоалкенов. Кинетика реакции в этом случае обычно описывается более простым уравнением второго порядка v = k[алкен], т. е. соответствует бимолекулярному Ad E 2-механизму. Ad E 2-Механизм предполагает образование ионной пары, включающей карбокатион и галогенид-ион.

Нельзя ожидать, что механизм присоединения с участием ионных пар будет отличаться высокой стереоселективностью. Если ионная пара превращается в конечный продукт быстрее, чем происходит вращение вокруг простой углерод-углеродной связи, конечным результатом будет син -присоединение, где протон и галогенид-ион присоединяется с одной и той же стороны двойной связи. В противном случае наблюдается образование продуктов как син - так и анти -присоединения НХ. Такой случай реализуется при гидрогалогенировании пара -замещенных стиролов Z-C 6 H 4 -CH=CH 2 . Наблюдаемая здесь закономерность заключается в том, что син -присоединение характерно лишь для тех олефинов, которые при протонировании дают относительно стабильный карбокатион, т. е. в случае донорных заместителей Z.
Для реакций гидрогалогенирования, протекающих по Ad E 2-механизму характерна конкуренция процессов сопряженного присоединения и перегруппировок, поскольку в качестве интермедиата образуется карбокатион или ионная пара.

В качестве примера перегруппировок с 1,2-миграцией алкильной группы и гидрид-иона приведем реакции гидрогалогенирования соответственно трет-бутилэтилена и изопропилэтилена.

При проведении этой же реакции без растворителя на холоду (-78 0 С) образуется смесь 33% нормального и 67% аномального (перегруппированного) продуктов присоединения.

4.3.в. Ориентация. Правило Марковникова
В отличие от симметричных электрофилов (Hal 2), галогеноводороды представляют собой несимметричные электрофильные реагенты. Присоединение любого несимметричного электрофила (HBr, ICl, H 2 O, Hg(OAc) 2 и т. д.) к несимметричному алкену в принципе могло бы дать смесь двух альтернативных продуктов, однако на практике обычно образуется только один из них. В качестве примера рассмотрим присоединение бромистого водорода к пропилену.

Еще в 1870 г. В.В. Марковников сформулировал эмпирическое правило, согласно которому несимметричные алкены присоединяют НХ таким путем, что преимущественно образуется продукт, в котором водород присоединяется к наименее замещенному, а Х - к наиболее замещенному концу двойной связи.
Обычно правило Марковникова объясняют различием в стабильности двух альтернативных карбокатионов. Например, в приведенном выше примере нормальный н -пропильный катион значительно менее стабилен, чем изопропильный катион, и поэтому реакция идет по второму пути.
Правило Марковникова первоначально использовалось только для случаев присоединения НХ к углеводородным субстратам, но в принципе его можно распространить и на реакции других замещенных алкенов. Так, присоединение НCl к CF 3 CH=CH 2 дает "анти -марковниковский" продукт CF 3 CH 2 CH 2 Cl. Этого и следовало ожидать, поскольку катион CF 3 CH+ CH 3 менее стабилен, чем катион CF 3 CH 2 CH 2+ из-за сильного (-I)-эффекта CF 3 -группы. Преимущественно образуется катион CF 3 CH 2 CH 2+ , но он тоже, хотя и в меньшей степени дестабилизирован индуктивным эффектом CF 3 -группы, вследствие чего присоединение HCl к трифторметилэтилену идет значительно медленнее, чем присоединение к незамещенному этилену.
По аналогичной причине катионы винилтриалкиламмония присоединяют HBr также против правила Марковникова:
Присоединение НХ к алкенам, имеющим сильные (-I) и (-M)-заместители, например, к акрилонитрилу или нитроэтилену также должно идти против правила Марковникова. Однако в этом случае двойная связь настолько сильно дезактивирована по отношению к электрофильным реагентам, что эти реакции идут лишь в очень жестких условиях. Хлористый винил СН 2 =СНСl всегда дает исключительно "марковниковские аддукты". Например, при его реакции с HCl образуется только 1,1-дихлорэтан (геминальный дихлорид) CH 3 CHCl 2 . Хлор, аналогично CF 3 -группе имеет сильный (-I)-эффект, и на первый взгляд, кажется, что по этой причине присоединение должно иметь антимарковниковскую ориентацию, т. к. катион + CH 2 CH 2 Cl должен быть более стабильным, чем катион СН 3 СН + Cl. Однако, в отличие от CF 3 -группы, хлор кроме (-I)-эффекта обладает также противодействующим ему (+М)-эффектом (т. к. имеет неподеленные пары). Опыт показывает, что величина мезомерного эффекта вполне достаточна, чтобы понизить энергию 1-хлорэтильного катиона ниже уровня энергии 2-хлорэтильного катиона, в котором +М-эффект не проявляется.
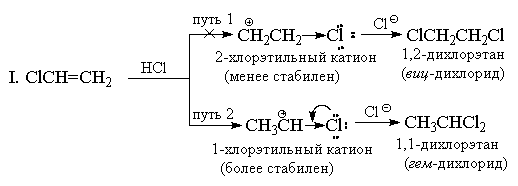
II. С позиций теории резонанса строение 1-хлорэтильного катиона может быть представлено следующим образом:
Тем не менее, присоединение к хлористому винилу происходит медленнее, чем к этилену в тех же условиях, т. е. по суммарному эффекту (-I > +M) хлор остается электроноакцепторным заместителем по сравнению с водородом, а 1-хлорэтильный катион менее стабилен, чем С 2 Н 5 + . Аналогичным образом реагируют с НХ и другие винилгалогениды.
Виниловые эфиры CH 2 =CHOR присоединяют НХ (X=Hal) по правилу Марковникова с гораздо большей скоростью, чем все перечисленные выше замещенные алкены. Это связано со значительным +М-эффектом RО-группы. В отличие от атома хлора, RО-группа по суммарному электронному эффекту (+М > -I) является сильным электронодонорным заместителем, эффективно стабилизирующим соседний карбокатионный центр. Строение карбокатиона в этом случае также может быть представлено в виде набора двух резонансных структур
Атака оксониевого катиона галогенид-анионом приводит к образованию -галогенэфиров типа СН 3 СН(Hal)OR.
4.3.г. Гидратация алкенов
Кислотно-катализируемая гидратация алкенов приводит к образованию спиртов. Направление гидратации алкенов определяется правилом Марковникова, поэтому предполагается, что в качестве промежуточной частицы в этой реакции образуется карбокатион.
Склонность вторичных алкильных карбокатионов к перегруппировкам мешает использованию гидратации алкенов для получения вторичных спиртов.

Этот метод в лаборатории нашел ограниченную область применения только для получения третичных спиртов. Реакция гидратации в этом случае в значительной степени обратима и третичные спирты образуются с низкими выходами (40-45%).


Гидратация простейших алкенов - этилена и пропилена - представляет собой важный промышленный метод получения этилового и изопропилового спиртов.

В лабораторной практике прямая гидратация алкенов не нашла широкого применения как вследствие жестких условий, так и благодаря образованию значительного количества изомерных спиртов. В настоящее время для региоселективного получения спиртов из алкенов обычно используется родственная реакция гидроксимеркурирования - демеркурирования.
4.3.д. Гидроксимеркурирование-демеркурирование
Электрофильная атака на двойную связь алкена может осуществляться ионами металлов, среди которых особое положение занимает катион ртути (II). Ацетат ртути в очень мягких условиях при 20 0 С присоединяется к алкенам в водном тетрагидрофуране (ТГФ) или в водной уксусной кислоте с образованием ртутьорганических соединений. Присоединение ацетата ртути по двойной связи протекает региоспецифично в строгом соответствии с правилом Марковникова, т. е. катион ртути присоединяется к наименее замещенному атому углерода.
Связь С-Hg в ртутьорганических соединениях может быть легко расщеплена под действием боргидрида натрия NaBH 4 , с образованием ртути и новой связи С-Н. Предполагается, что в качестве нестабильного интермедиата при этом получается алкилмеркургидрид, который далее разлагается с выделением металлической ртути по радикальному механизму.

Суммарно этот двухстадийный процесс гидроксимеркурирования-демеркурирования в конечном итоге представляет собой региоспецифичную гидратацию алкена по правилу Марковникова в исключительно мягких условиях, когда образование побочных продуктов сведено к предельно возможному минимуму. Это можно наглядно проиллюстрировать с помощью следующих примеров, в которых суммарный выход продуктов реакции составляет 90-98%. Приведенные цифровые данные в этом случае обозначают не выходы образующихся соединений, а их соотношение в смеси.
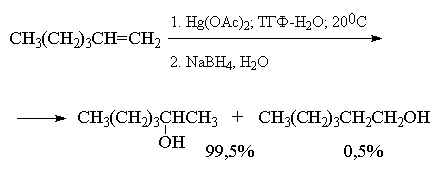



Как видно из приведенных выше примеров гидроксимеркурирование-демеркурирование алкенов в большинстве случаев обеспечивает региоспецифическую гидратацию алкенов с образованием практически только одного из двух изомерных спиртов. Следует отметить, что нет никакой необходимости в выделении ртутьорганического соединения, и оба процесса могут быть проведены непосредственно один за другим.
Гидроксимеркурирование несимметричных алкенов, по-видимому, начинается с атаки катиона AcOHg + и образования в качестве интермедиата несимметричного циклического меркуриниевого катиона (аналога несимметричного галогенониевого иона), который затем раскрывается в результате нуклеофильной атаки водой по наиболее замещенному атому углерода, несущему больший положительный заряд.

Мостиковый меркуриниевый ион можно зафиксировать в ненуклеофильной сильнокислой среде даже при 20 0 С при присоединении более сильного электрофильного агента - трифторацетата ртути в смеси фторсульфоновой кислоты и пятифтористой сурьмы.

Меркуриниевый катион может расщепляться не только при действии воды, но и других электронодонорных растворителей: спиртов, уксусной кислоты, ацетонитрила и др. Конечным продуктом реакции в этом случае будут соответственно простые эфиры, ацетаты или N-замещенные амиды уксусной кислоты, например:
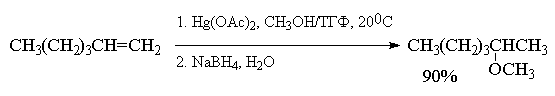

При использовании в реакции алкоксимеркурирования-демеркурирования разветвленных вторичных или третичных спиртов более эффективными, чем ацетат ртути, являются трифторацетат Hg(OCOCF 3) 2 или трифлат ртути Hg(OSO 2 CF 3) 2 .

Таким образом, гидрокси- и алкоксимеркурирование-демеркурирование - это один из лучших препаративных методов синтеза спиртов и простых эфиров с разветвленными алкильными радикалами.
Присоединение солей ртути к алкенам представляет собой наиболее яркий пример реакции сопряженного присоединения к двойной связи, где роль внешнего нуклеофильного агента выполняет растворитель. Стереохимия двойного процесса гидроксимеркурирования-демеркурирования зависит от стереохимического результата каждой отдельной стадии. Для гидроксимеркурирования характерно анти -присоединение, как и для других реакций с участием циклического катиона. Однако радикальное демеркурирование не отличается высокой стереоселективностью. Поэтому весь процесс в целом также нестереоспецифичен.
4.3.е. Присоединение алкенов (катионная димеризация и полимеризация алкенов)
Наиболее интересным примером такого типа реакций является димеризация и полимеризация изобутилена в присутствии серной кислоты.

Техническое название этой смеси алкенов - "диизобутилен". Данная реакция протекает по катионному механизму, сходному с механизмом присоединения минеральных кислот к двойной связи алкенов. На первой стадии протон присоединяется к молекуле изобутилена с образованием относительно стабильного трет -бутилкатиона. Далее образовавшийся трет -бутилкатион (кислота Льюиса) реагирует с молекулой изобутилена (основание Льюиса) с образованием нового стабильного третичного октильного катиона.
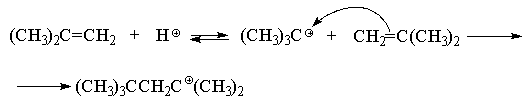
В данных условиях под действием оснований (H 2 O, HSO 4 - -ионы) октильный карбокатион быстро теряет протон и превращается в смесь изомерных пентенов, т. к. отрыв протона происходит из двух различных положений:

Преимущественное образование термодинамически менее стабильного алкена - 2,4,4-триметилпентена-1 (80% в реакционной смеси) связано с большей пространственной доступностью для атаки основанием атомов водорода метильных групп, по сравнению с атомами водорода метиленовой группы. В промышленности "диизобутилен" гидрируют на Ni-Ренея и получают "изооктан" (техническое название углеводорода 2,2,4-триметилпентана), используемый в качестве высокооктанового топлива для двигателей внутреннего сгорания.
При высоких концентрациях серной кислоты (более 80%) происходит катионная полимеризация изобутилена с образованием полимера, называемого полиизобутиленом (-CH 2 C(CH 3) 2 -) n . Этот каучукоподобный полимер используют для получения антикоррозионных и гидроизоляционных покрытий, герметиков и др.
Кроме изобутилена, по катионному механизму полимеризуются 3-метилбутен-1, виниловые эфиры и некоторые производные стирола, способные образовывать сравнительно устойчивые карбокатионы. В качестве катализаторов катионной полимеризации также используют фтористый водород и кислоты Льюиса: BF 3 , AlCl 3 , AlBr 3 и др. в присутствии очень малых количеств воды.
4.3.ж. Присоединение алканов (алкилирование алкенов)
Другой промышленный метод синтеза "изооктана" основан на взаимодействии изобутилена с избытком изобутана в присутствии концентрированной серной кислоты или в безводном фтористом водороде при 0 10 0 С.

Эта реакция также протекает по катионному механизму и, что особенно интересно, является примером цепного катионного процесса. Сначала изобутилен в условиях реакции димеризуется с образованием третичного октильного катиона (CH 3) 3 CCH 2 C + (CH 3) 2 . Подробно механизм его образования изложен в предыдущем разделе. Далее происходит быстрый перенос водорода (в виде гидрид-иона) от изобутана к октильному катиону с образованием молекулы "изооктана" и нового трет-бутилкатиона, который в свою очередь быстро реагирует с изобутиленом с образованием нового октильного катиона и т. д.

Кроме синтеза "изооктана", такой метод алкилирования используется в нефтехимической промышленности для синтеза высококипящих разветвленных углеводородов из разветвленных алкенов и алканов низкокипящих фракцией термического крекинга.
Алкены ненасыщенные алифатические углеводороды с одной или несколькими двойными углерод-углеродными связями. Двойная связь превращает два атома углерода в плоскую структуру с валентными углами между соседними связями по 120°С:
Гомологический ряд алкенов имеет общую формулу двумя его первыми членами являются этен (этилен) и пропен (пропилен):

Члены ряда алкенов с четырьмя или большим числом атомов углерода обнаруживают изомерию положения связей. Например, алкен с формулой имеет три изомера, два из которых являются изомерами положения связей:
Заметим, что нумерация цепи алкенов производится с того ее конца, который ближе к двойной связи. Положение двойной связи указывается меньшим из двух номеров, которые соответствуют двум атомам углерода, связанным между собой двойной связью. Третий изомер имеет разветвленную структуру:

Число изомеров какого-либо алкена возрастает с числом атомов углерода. Например, гексен имеет три изомера положения связей:
диенов является бута-1,3-диен, или просто бутадиен:
Соединения, содержащие три двойные связи, называются триенами. Соединения с несколькими двойными связями имеют общее название полиены.
Физические свойства
Алкены имеют несколько более низкие температуры плавления и кипения, чем соответствующие им алканы. Например, пентан имеет температуру кипения . Этилен, пропен и три изомера бутена при комнатной температуре и нормальном давлении находятся в газообразном состоянии. Алкены с числом атомов углерода от 5 до 15 в нормальных условиях находятся в жидком состоянии. Их летучесть, как и у алканов, возрастает при наличии разветвления в углеродной цепи. Алкены с числом атомов углерода больше 15 при нормальных условиях представляют собой твердые вещества.
Получение в лабораторных условиях
Двумя основными способами получения алкенов в лабораторных условиях являются дегидратация спиртов и дегидрогалогенирование галогеноалканов. Например, этилен можно получить дегидратацией этанола при действии избытка концентрированной серной кислоты при температуре 170 °С (см. разд. 19.2):
Этилен можно также получить из этанола, пропуская пары этанола над поверхностью нагретого оксида алюминия. Для этой цели можно использовать установку, схематически изображенную на рис. 18.3.
Второй распространенный метод получения алкенов основан на проведении дегидрогалогенирования галогеноалканов в условиях основного катализа
Механизм реакции элиминирования такого типа описан в разд. 17.3.
Реакции алкенов
Алкены обладают намного большей реакционной способностью, чем алканы. Это обусловлено способностью -электронов двойной связи притягивать электрофилы (см. разд. 17.3). Поэтому характерные реакции алкенов представляют собой главным образом реакции электрофильного присоединения по двойной связи:

Многие из этих реакций имеют ионные механизмы (см. разд. 17.3).
Гидрирование
Если какой-нибудь алкен, например этилен, смешать с водородом и пропустить эту смесь над поверхностью платинового катализатора при комнатной температуре или никелевого катализатора при температуре около 150°С, то произойдет присоединение
водорода по двойной связи алкена. При этом образуется соответствующий алкан:

Реакция этого типа представляет собой пример гетерогенного катализа. Его механизм описан в разд. 9.2 и схематически показан на рис. 9.20.
Присоединение галогенов
Хлор или бром легко присоединяются по двойной связи алкена; эта реакция протекает в неполярных растворителях, например в тетрахлорометане или гексане. Реакция протекает по ионному механизму, который включает образование карбкатиона. Двойная связь поляризует молекулу галогена, превращая ее в диполь:

Поэтому раствор брома в гексане или тетрахлорометане при встряхивании с алкеном обесцвечивается. То же самое происходит, если встряхивать алкен с бромной водой. Бромная вода представляет собой раствор брома в воде. Этот раствор содержит бромноватистую кислоту . Молекула бромноватистой кислоты присоединяется по двойной связи алкена, и в результате образуется бромозамещенный спирт. Например

Присоединение галогеноводородов
Механизм реакции этого типа описан в разд. 18.3. В качестве примера рассмотрим присоединение хлороводорода к пропену:
Отметим, что продукт этой реакции представляет собой 2-хлоропропан, а не 1-хлоро-пропан:
![]()
В таких реакциях присоединения наиболее электроотрицательный атом или наиболее электроотрицательная группа всегда присоединяются к атому углерода, связанному с
наименьшим числом атомов водорода. Эта закономерность носит название правила Марковникова.
Предпочтительное присоединение электроотрицательного атома или группы к атому углерода, связанному с наименьшим числом атомов водорода, обусловлено повышением устойчивости карбкатиона по мере возрастания числа алкильных заместителей на атоме углерода. Это повышение устойчивости в свою очередь объясняется индуктивным эффектом, возникающим в алкильных группах, так как они являются донорами электронов:

В присутствии какого-либо органического пероксида пропен реагирует с бромоводородом, образуя т. е. не по правилу Марковникова. Такой продукт называется антимарковниковским. Он образуется в результате протекания реакции по радикальному, а не ионному механизму.
Гидратация
Алкены реагируют с холодной концентрированной серной кислотой, образуя алкил-гидросульфаты. Например

Эта реакция представляет собой присоединение, поскольку в ней происходит присоединение кислоты по двойной связи. Она является обратной реакцией по отношению к дегидратации этанола с образованием этилена. Механизм этой реакции подобен механизму присоединения галогеноводородов по двойной связи. Он включает образование промежуточного карбкатиона. Если продукт этой реакции разбавить водой и осторожно нагревать, он гидролизуется, образуя этанол:
Реакция присоединения серной кислоты к алкенам подчиняется правилу Марковникова:

Реакция с подкисленным раствором перманганата калия
Фиолетовая окраска подкисленного раствора перманганата калия исчезает, если этот раствор встряхивают в смеси с каким-либо алкеном. Происходит гидроксилирование алкена (введение в него гидроксигруппы, образующейся вследствие окисления), который в результате превращается в диол. Например, при встряхивании избыточного количества этилена с подкисленным раствором происходит образование этан-1,2-диола (этиленгликоля)

Если алкен встряхивают с избыточным количеством раствора -ионов, происходит окислительное расщепление алкена, приводящее к образованию альдегидов и кетонов:
Альдегиды, образующиеся при этом, подвергаются дальнейшему окислению с образованием карбоновых кислот.
Гидроксилирование алкенов с образованием диолов может также проводиться с помощью щелочного раствора перманганата калия.
Реакция с пербензойной кислотой
Алкены реагируют с пероксикислотами (надкислотами), например с пербензойной кислотой, образуя простые циклические эфиры (эпоксисоединения). Например

При осторожном нагревании эпоксиэтана с разбавленным раствором какой-либо кислоты образуется этан-1,2-диол:

Реакции с кислородом
Как и все другие углеводороды, алкены горят и при обильном доступе воздуха образуют диоксид углерода и воду:
При ограниченном доступе воздуха горение алкенов приводит к образованию моноксида углерода и воды:
Поскольку алкены имеют более высокое относительное содержание углерода, чем соответствующие алканы, они горят с образованием более дымного пламени. Это обусловлено образованием частиц углерода:
Если смешать какой-либо алкен с кислородом и пропустить эту смесь над поверхностью серебряного катализатора, при температуре около 200 °С образуется эпоксиэтан:
Озонолиз
При пропускании газообразного озона через раствор какого-либо алкена в трихлорометане или тетрахлорометане при температуре ниже 20 °С образуется озонид соответствующего алкена (оксиран)

Озониды - неустойчивые соединения и могут быть взрывоопасными. Они подвергаются гидролизу с образованием альдегидов или кетонов. Например

В этом случае часть метаналя (формальдегида) реагирует с пероксидом водорода, образуя метановую (муравьиную) кислоту:
Полимеризация
Простейшие алкены могут полимеризоваться с образованием высокомолекулярных соединений, которые обладают той же эмпирической формулой, что и исходный алкен:
Эта реакция протекает при высоком давлении, температуре 120°С и в присутствии кислорода, который играет роль катализатора. Однако полимеризацию этилена можно проводить и при более низком давлении, если воспользоваться катализатором Циглера. Одним из наиболее распространенных катализаторов Циглера является смесь триэтилалюминия и тетрахлорида титана.
Полимеризация алкенов более подробно рассматривается в разд. 18.3.