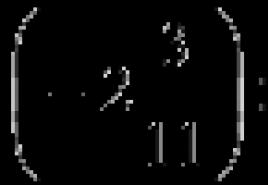Общая формула алкенов следующая. Физические свойства алкенов, применение, способы получения
Первым представителем ряда алкенов является этен (этилен), чтобы построить формулу следующего представителя ряда нужно к исходной формуле прибавить группу CH 2 ; многократно повторяя такую процедуру можно построить гомологический ряд алкенов.
CH 2 +CH 2 +CH 2 +CH 2 +CH 2 +CH 2 +CH 2 +CH 2
C 2 H 4 ® C 3 H 6 ® C 4 H 8 ® C 5 H 10 ® C 6 H 12 ® C 7 H 14 ® C 8 H 16 ® C 9 H 18 ® C 10 H 20
Чтобы построить название алкена необходимо в названии соответствующего алкана (с таким же числом атомов углерода как ив алкене) поменять суффикс – ан на - ен (или – илен).Например, алкан с четырьмя атомами углерода в цепи называется бутан, а соответствующий ему алкен – бутен (бутилен). Исключение составляет декан, соответствующий ему алкен будет называться не декен, а децен (децилен). Алкен с пятью атомами углерода в цепи помимо названия пентен имеет название амилен. В таблице ниже приведены формулы и названия первых десяти представителей ряда алкенов.
Однако, начиная с третьего, представитель ряда алкенов – бутена помимо словесного названия «бутен» после его написания должна стоять цифра 1 или 2, которая показывает местоположение двойной связи в углеродной цепи.
CH 2 = CH – CH 2 – CH 3 CH 3 – CH = CH – CH 3
бутен 1 бутен 2
Помимо систематической номенклатуры часто употребляются и рациональные названия алкенов при этом алкены рассматриваются, как производные этилена, в молекуле которого атомы водорода замещены на радикалы, а за основу берется название «этилен».
Например, CH 3 – CH = CH – C 2 H 5 – симметричный метилэтилэтилен.
(СH 3) – CH = CH – C 2 H 5 – симметричный этилизопропилэтилен.
(СH 3)C – CH = CH – CH(CH 3) 2 – симметричный изопропилизобутилэтилен.
Непредельные углеводородные радикалы по систематической номенклатуре называют, добавляя к корню суффикс - енил : этенил
CH 2 =CH -, пропенил-2 CH 2 = CH – CH 2 - . Но гораздо чаще для этих радикалов употребляют эмпирические названия – соответственно винил и аллил .
Изомерия алкенов.
Для алкенов характерно большое количество разных видов изомерии.
А) Изомерия углеродного скелета.
CH 2 = C – CH 2 – CH 2 – CH 3 СH 2 = CH – CH – CH 2 – CH 3
2-метил пентен-1 3-метил пентен-1
СH 2 = CH – CH 2 – CH – CH 3
4- метил пентен-1
Б) Изомерия положения двойной связи.
СH 2 = СH – CH 2 – CH 3 CH 3 – CH = CH – CH 3
бутен-1 бутен-2
В) Пространственная (стереоизомерия).
Изомеры, у которых одинаковые заместители расположены по одну сторону от двойной связи, называют цис -изомеры, а по разную – транс -изомерами:
H 3 C CH 3 H 3 C H
цис -бутен транс -бутен
Цис - и транс - изомеры отличаются не только пространственным строением, но и многими физическими и химическими (и даже физиологическими) свойствами. Транс - Изомеры более устойчивы по сравнению с цис-изомерами . Это объясняется большей удаленностью в пространстве групп при атомах, связанных двойной связью, в случае транс – изомеров.
Г) Изомерия веществ разных классов органических соединений.
Изомерами алкенам являются циклопарафины, имеющие сходную с ними общую формулу – С n H 2 n .
CH 3 – CH = CH – CH 3
бутен -2
циклобутан
4. Нахождение алкенов в природе и способы их получения.
Также как и алканы, алкены в природе встречаются в составе нефти, попутного нефтяного и природного газов, бурого и каменного угля горючих сланцев.
А) Получение алкенов каталитической дегидрогенизацией алканов.
СH 3 – CH – CH 3 ® CH 2 = C – CH 3 + H 2
CH 3 кат. (K 2 O-Cr 2 O 3 -Al 2 O 3) CH 3
Б) Дегидратация спиртов под действием серной кислоты или с участием Al 2 O 3 (парафазная дегидратация).
этанол H 2 SO 4 (конц.) этен
C 2 H 5 OH ® CH 2 = CH 2 + H 2 O
этанол Al 2 O 3 этен
Дегидратация спиртов протекает по правилу А.М. Зайцева, согласно которому водород отщепляется от наименее гидрогенезированного атома углерода, то есть вторичного или третичного.
H 3 C – CH – C ® H 3 C – CH = C – CH 3
3-метилбутанол-2 2-метилбутен
В) Взаимодействие галогеналкилов со щелочами (дегидрогалогенирование).
H 3 C – C – CH 2 Cl + KOH ® H 3 C – C = CH 2 + H 2 O + KCl
1-хлор 2-метлпропан (спирт. р-р) 2-метилпропен-1
Г) Действие магнием или цинком на дигалогенпроизводные алкилов с атомами галогена при соседних углеродных атомах (дегалогенирование).
спирт. t
CH 3 -CHCl-CH 2 Cl + Zn ® CH 3 -CH = CH 2 + ZnCl 2
1.2- дихлорпропан пропен-1
Д) Селективное гидрирование алкинов на катализаторе.
СH º CH + H 2 ® CH 2 =CH 2
этин этен
5. Физические свойства алкенов.
Первые три представителя гомологического ряда этилена газы.
Начиная с C 5 H 10 до С 17 Н 34 – жидкости, начиная с С 18 Н 36 и далее твердые вещества. С увеличением молекулярной массы повышаются температуры плавления и кипения. Алкены с углеродной цепью нормального строения кипят при более высокой температуре, чем их изомеры, имеющие изостроение. Температура кипения цис - изомеров выше, чем транс – изомеров, а температура плавления – наоборот. Алкены малополярны, но легко поляризуются. Алкены плохо растворимы в воде (однако лучше, чем соответствующие алканы). Они хорошо растворяются в органических растворителях. Этилен и пропилен горят кипящим пламенем.
В таблице ниже приведены основные физические свойства некоторых представителей ряда алкенов.
| Алкен | Формула | t пл. o C | t кип. o C | d 4 20 |
| Этен (этилен) | C 2 H 4 | -169,1 | -103,7 | 0,5700 |
| Пропен (пропилен) | C 3 H 6 | -187,6 | -47,7 | 0,6100 (при t(кип) ) |
| Бутен (бутилен-1) | C 4 H 8 | -185,3 | -6,3 | 0,5951 |
| цис – Бутен-2 | C 4 H 8 | -138,9 | 3,7 | 0,6213 |
| транс – Бутен-2 | C 4 H 8 | -105,5 | 0,9 | 0,6042 |
| Изобутилен (2-метилпропен) | C 4 H 8 | -140,4 | -7,0 | 0,6260 |
| Пентен-1 (амилен) | C 5 H 10 | -165,2 | +30,1 | 0,6400 |
| Гексен-1 (гексилен) | C 6 H 12 | -139,8 | 63,5 | 0,6730 |
| Гептен-1 (гептилен) | C 7 H 14 | -119 | 93,6 | 0,6970 |
| Октен-1 (октилен) | C 8 H 16 | -101,7 | 121,3 | 0,7140 |
| Нонен-1 (нонилен) | C 9 H 18 | -81,4 | 146,8 | 0,7290 |
| Децен-1 (децилен) | C 10 H 20 | -66,3 | 170,6 | 0,7410 |
6. Химические свойства алкенов.
А) Присоединение водорода (гидрирование).
CH 2 = CH 2 + H 2 ® CH 3 – CH 3
этен этан
Б)Взаимодействие с галогенами (галогенирование).
Легче идет присоединение хлора и брома к алкенам, труднее - йода
CH 3 – CH = CH 2 + Cl 2 ® CH 3 – CHCl – CH 2 Cl
пропилен 1,2-дихлорпропан
В) Присоединение галогенводородов (гидрогалогенирование)
Присоединение галогенводородов к алкенам при обычных условиях протекает согласно правилу Марковникова: при ионном присоединении галогенводородов к несимметричным алкенам (при обычных условиях) водород присоединяется по месту двойной связи к наиболее гидрогенизированному (связанному с наибольшим числом водородных атомов)атому углерода, а галоген – менее гидрогенизированному.
CH 2 =CH 2 + HBr ® CH 3 – CH 2 Br
этен бромэтан
Г) Присоединение воды к алкенам (гидратация).
Присоединение воды к алкенам протекает также согласно правилу Марковникова.
CH 3 – CH = CH 2 + H – OH ® CH 3 – CHOH – CH 3
пропен-1 пропанол-2
Е) Алкилирование алканов алкенами.
Алкилирование – реакция, с помощью которой можно вводить различные углеводородные радикалы (алкилы) в молекулы органических соединений. В качестве алкилирующих средств используют галогеналкилы, непредельные углеводороды, спирты и другие органические вещества. Например, в присутствии концентрированной серной кислоты активно протекает реакция алкилирования изобутана изобутиленом:
3CH 2 = CH 2 + 2KMnO 4 + 4H 2 O ® 3CH 2 OH – CH 2 OH + 2MnO 2 + 2KOH
этен этиленгликоль
(этандиол-1,2)
Расщепление молекулы алкена по месту двойной связи может вести к образованию соответствующей карбоновой кислоты, если используется энергичный окислитель (азотная концентрированная кислота или хромовая смесь).
HNO 3(конц.)
CH 3 – CH = CH – CH 3 ® 2CH 3 COOH
бутен-2 этановая кислота (уксусная кислота)
Окисление этилена кислородом воздуха в присутствии металлического серебра ведёт к образованию этиленоксида.
2CH 2 = CH 2 + O 2 ® 2CH 2 – CH 2
И) Реакция полимеризации алкенов.
n CH 2 = CH 2 ® [–CH 2 – CH 2 –]n
этилен кат.полиэтилен
7.Применение алкенов.
А) Резка и сварка металлов.
Б) Производство красителей, растворителей, лаков, новых органических веществ.
В) Производство пластмасс и других синтетических материалов.
Г) Синтез спиртов, полимеров, каучуков
Д) Синтез лекарственных препаратов.
IV. Диеновые углеводороды (алкадиены или диолефины) – это непредельные сложные органические соединения с общей формулой C n H 2 n -2 , содержащие две двойные связи между атомами углерода в цепи и способные присоединять молекулы водорода, галогенов и других соединений в силу валентной не насыщенности атома углерода.
Первым представителем ряда диеновых углеводородов является пропадиен (аллен). Строение диеновых углеводородов сходно со строением алкенов, разница лишь только в том, что в молекулах диеновых углеводородов две двойные связи, а не одна.
Для алкенов характерны, прежде всего, реакции присоединения по двойной связи. В основном эти реакции идут по ионному механизму. Пи-связь разрывается, и образуются две новые сигма-связи. Напомню, что для алканов типичными были реакции замещения и шли они по радикальному механизму. Присоединяться к алкенам могут молекулы водорода, эти реакции называются гидрирование, молекулы воды, гидратация, галогены галогенирование, галогенводороды гидрогалогенирование. Но обо всем по порядку.
Реакции присоединения по двойной связи
Итак, первое химическое свойство способность присоединять галогеноводороды, гидрогалогенирование.
Пропен и остальные алкены реагируют с галогеноводородами по правилу Марковникова.

Атом водорода присоединяется к наиболее гидрированному, или правильнее сказать гидрогенизированному, атому углерода.
Вторым номером в нашем списке свойств будет гидратация, присоединение воды.
Реакция проходит при нагревании в присутствии кислоты обычно серной или фосфорной. Присоединение воды происходит также по правилу Марковникова, то есть первичный спирт можно получить только гидратацией этилена, остальные неразветвленные алкены дают вторичные спирты.

И для гидрогалогениерования и для гидратации существуют исключения из правила Марковникова. Во-первых, против этого правила присоединение протекает в присутствии пероксидов.
Во-вторых, для производных алкенов, в которых присуствуют электронноакцепторне группы. Например, для 3,3,3-трифторпропена-1.

Атомы фтора за счет высокой электроотрицательности оттягивают на себя электронную плотность по цепи сигма-связей. Такое явление называется отрицательным индуктивным эффектом.

Из-за этого происходит смещение подвижных пи-электронов двойной связи и у крайнего атома углерода оказывается частичный положительный заряд, который обычно обозначается как дельта плюс. Именно к нему и пойдет отрицательно заряженный ион брома, а катион водорода присоединится к наименее гидрированному атому углерода.
Помимо трифторметильной группы отрицательным индуктивным эффектом обладает, например, трихлорметильная группа, нитрогруппа, карбоксильная группа и некоторые другие.
Этот второй случай нарушения правила Марковникова в ЕГЭ встречается очень редко, но все-таки желательно иметь его в виду, если вы планируете сдать экзамен на максимальный балл.
Третье химическое свойство присоединение молекул галогенов.
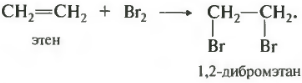
В первую очередь это касается брома, поскольку данная реакция является качественной на кратную связь. При пропускании, например, этилена через бромную воду, то есть раствор брома в воде, имеющий коричневый цвет, происходит ее обесцвечивание. Если пропускать через бромную воду смесь газов, например, этан и этен, то можно получить чистый этан без примеси этена, поскольку тот останется в реакционной колбе в виде дибромэтана, представляющего собой жидкость.
Особым образом стоит отметить реакцию алкенов в газовой фазе при сильном нагревании, например, с хлором.
При таких условиях протекает не реакция присоединения, а реакция замещения. При чем исключительно по альфа-атому углерода, то есть атому, соседствующему с двойной связью. В данном случае получается 3-хлорпропен-1. Эти реакции на экзамене встречаются нечасто, поэтому большинство учеников их не помнит и, как правило, совершает ошибки.
Четвертым номером идет реакция гидрирования, а вместе с ней и реакция дегидрирования. То есть присоединение или отщепление водорода.
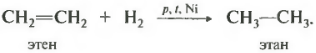
Гидрирование происходит при не очень высокой температуре на никелевом катализаторе. При более высокой температуре возможно дегидрирование с получением алкинов.
Пятым свойством алкенов является способность к полимеризации, когда сотни и тысячи молекул алкена за счет разрыва пи-связи и образования сигма-свзяей друг с другом образуют очень длинные и прочные цепочки.
В данном случае получился полиэтилен. Обратите внимание, что в получившейся молекуле кратные связи отсутствуют. Такие вещества называются полимерами, исходные молекулы называются мономерами, повторяющийся фрагмент это элементарное звено полимера, а число n степень полимеризации.
Также возможны реакции получения других важных полимерных материалов, например, полипропилена.


Еще один важный полимер поливинилхлорид.

Исходным веществом для производства этого полимера является хлорэтен, тривиальное название которого винилхлорид. Поскольку этот непредельный заместитель называется винил. Часто встречающаяся аббревиатура на пластмассовых изделиях ПВХ как раз расшифровывается как поливинилхлорид.
Мы обсудили пять свойств, которые представляли собой реакции присоединения по двойной связи. Теперь обратимся к реакциям окисления .
Реакции окисления алкенов
Шестое химическое свойство в нашем общем списке это мягкое окисление или реакция Вагнера. Оно протекает при воздействии на алкен водным раствором перманганата калия на холоду, поэтому часто в экзаменационных заданиях указывают температуру ноль градусов.
В результате получается двухатомный спирт. В данном случае этиленгликоль, а в целом такие спирты носят общее название гликоли. В процессе реакции фиолетово-розовый раствор перманганата обесцвечивается, поэтому эта реакция также является качественной на двойную связь. Марганец в нейтральной среде из степени окисления +7 восстанавливается до степени окисления +4. Рассмотрим еще несколько примеров. УРАВНЕНИЕ
Здесь получился пропандиол-1,2. Однако таким же образом будут реагировать и циклические алкены. УРАВНЕНИЕ
Еще один вариант, когда двойная связь находится, например, в боковой цепи ароматических углеводородов. Регулярно в заданиях егэ встречается реакция Вагнера с участием стирола, его второе название винилбензол.
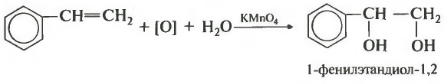
Я надеюсь, что представил вашему вниманию достаточно примеров, чтобы вы поняли, что мягкое окисление двойной связи всегда подчиняется довольно простому правилу пи-связь разрывается и к каждому атому углерода присоединяется гидроксигруппа.
Теперь, что касается жесткого окисления. Это будет наше седьмое свойство. Такое окисление происходит, когда алкен реагирует с кислотным раствором перманганата калия при нагревании.
Происходит деструкция молекулы, то есть ее разрушение по двойной связи. В случае бутена-2 получились две молекулы уксусной кислоты. В целом же, по продуктам окисления можно судить о положении кратной связи в углеродной цепи.
При окислении бутена-1 получается молекула пропионовой (пропановой) кислоты и углекислый газ.
В случае этилена получится две молекулы углекислого газа. Во всех случаях в кислой среде марганец из степени окисления +7 восстанавливается до +2.
И, наконец, восьмое свойство полное окисление или горение.
Алкены сгорают, как и другие углеводороды, до углекислого газа и воды. Запишем уравнение сгорания алкенов в общем виде.
Молекул углекислого газа будет столько же, сколько и атомов углерода в молекуле алкена, поскольку в состав молекулы CO 2 входит один атом углерода. То есть n молекул CO 2 . Молекул воды будет в два раза меньше, чем атомов водорода, то есть 2n/2, а значит просто n.
Атомов кислорода слева и справа одинаковое количество. Справа их 2n из углекислого газа плюс n из воды, итого 3n. Слева атомов кислорода столько же, а значит молекул в два раза меньше, потому как в состав молекулы входят два атома. То есть 3n/2 молекул кислорода. Можно записать 1,5n.
Мы рассмотрели восемь химических свойств алкенов.
К непредельным относят углеводороды, содержащие в молекулах кратные связи между атомами углерода. Непредельными являются алкены, алкины, алкадиены (полиены) . Непредельным характером обладают также циклические углеводороды, содержащие двойную связь в цикле (циклоалкены ), а также циклоалканы с небольшим числом атомов углерода в цикле (три или четыре атома). Свойство «непредельности» связано со способностью этих веществ вступать в реакции присоединения, прежде всего водорода, с образованием предельных, или насыщенных углеводородов - алканов.
Строение алкенов
Ациклические углеводороды, содержащие в молекуле помимо одинарных связей, одну двойную связь между атомами углерода и соответствующие общей формуле СnН2n. Свое второе название - олефины
- алкены получили по аналогии с жирными непредельными кислотами (олеиновая, линолевая), остатки которых входят в состав жидких жиров - масел.
Атомы углерода, между которыми есть двойная связь, находятся в состоянии sр 2 -гибридизации. Это означает, что в гибридизации участвуют одна s- и две р-орбитали, а одна р-орбиталь остается негибридизованной. Перекрывание гибридных орбиталей приводит к образованию σ-связи, а за счет негибридизованных р-орбиталей
соседних атомов углерода образуется вторая, π-связь. Таким образом, двойная связь состоит из одной σ- и одной π — связи. Гибридные орбитали атомов, образующих двойную связь, находятся в одной плоскости, а орбитали, образующие π -связь, располагаются перпендикулярно плоскости молекулы. Двойная связь (0,132 им) короче одинарной, а ее энергия больше, т. к. она является более прочной. Тем не менее, наличие подвижной, легко поляризуемой π -связи приводит к тому, что алкены химически более активны, чем алканы, и способны вступать в реакции присоединения.

Строение этилена

Образование двойной связи в алкенах
Гомологический ряд этена
Неразветвленные алкены составляют гомологи- ческий ряд этена (этилена ): С 2 Н 4 - этен, С 3 Н 6 - пропен, С 4 Н 8 - бутен, С 5 Н 10 - пентен, С 6 Н 12 - гексен, С 7 Н 14 - гептен и т.д.
Изомерия алкенов
Для алкенов характерна структурная изомерия. Структурные изомеры отличаются друг от друга строением углеродного скелета. Простейший алкен, для которого характерны структурные изомеры, - это бутен:

Особым видом структурной изомерии является изомерия положения двойной связи:
Алкены изомерны циклоалканам (межклассовая изомерия), например:

Вокруг одинарной углерод-углеродной связи возможно практически свободное вращение атомов углерода, поэтому молекулы алканов могут приобретать самую разнообразную форму. Вращение вокруг двойной связи невозможно, что приводит к появлению у алкенов еще одного вида изомерии - геометрической, или цис- и транс- изомерии .


Цис-изомеры
отличаются от транс-изомеров
пространственным расположением фрагментов молекулы (в данном случае метильных групп) относительно плоскости π -связи, а следовательно, и свойствами.
Номенклатура алкенов
1. Выбор главной цепи.
Образование названия углеводорода начинается с определения главной цепи - самой длинной цепочки атомов углерода в молекуле. В случае алкенов главная цепь должна содержать двойную связь.
2. Нумерация атомов главной цепи.
Нумерация атомов главной цепи начинается с того конца, к которому ближе находится двойная связь.
Например,правильное название соединения:
![]()
Если по положению двойной связи нельзя определить начало нумерации атомов в цепи, то его определяет положение заместителей так же, как для предельных углеводородов.

3. Формирование названия. В конце названия указывают номер атома углерода, у которого начинается двойная связь, и суффикс -ен , обозначающий принадлежность соединения к классу алкенов. Например:

Физические свойства алкенов
Первые три представителя гомологического ряда алкенов - газы; вещества состава С5Н10 — С16Н32 - жидкости; высшие алкены - твердые вещества.
Температуры кипения и плавления закономерно повышаются при увеличении молекулярной массы соединений.
Химические свойства алкенов
Реакции присоединения
. Напомним, что отличительной чертой представителей непредельных углеводородов - алкенов является способность вступать в реакции присоединения. Большинство этих реакций протекает по механизму электрофильного присоединения
.
1. Гидрирование алкенов.
Алкены способны присоединять водород в присутствии катализаторов гидрирования, металлов - платины, палладия, никеля:
Эта реакция протекает при атмосферном и повышенном давлении и не требует высокой температуры, т. к. является экзотермической. При повышении температуры на тех же катализаторах может пойти обратная реакция - дегидрирование.
2. Галогенирование (присоединение галогенов)
. Взаимодействие алкена с бромной водой или раствором брома в органическом растворителе (СС14) приводит к быстрому обесцвечиванию этих растворов в результате присоединения молекулы галогена к алкену и образования дигалогеналканов.
3. Гидрогалогенирование (присоединение галогеноводорода)
.
Эта реакция подчиняется
При присоединении галогеноводорода к алкену водород присоединяется к более гидрированному атому углерода, т. е. атому, при котором находится больше атомов водорода, а галоген - к менее гидрированному.


4. Гидратация (присоединение воды).
Гидратация алкенов приводит к образованию спиртов. Например, присоединение воды к этену лежит в основе одного из промышленных способов получения этилового спирта.
Обратите внимание на то, что первичный спирт (с гидроксогруппой при первичном углероде) образуется только при гидратации этена. При гидратации пропена или других алкенов образуются вторичные спирты .

Эта реакция протекает также в соответствии с правилом Марковникова - катион водорода присоединяется к более гидрированному атому углерода, а гидроксогруппа - к менее гидрированному.
5. Полимеризация.
Особым случаем присоединения является реакция полимеризации алкенов:
Эта реакция присоединения протекает по свободнорадикальному механизму.
Реакции окисления.
1. Горение.
Как и любые органические соединения, алкены горят в кислороде с образованием СО2 и Н2О:
2. Окисление в растворах. В отличие от алканов алкены легко окисляются под действием растворов перманганата калия. В нейтральных или щелочных растворах происходит окисление алкенов до диолов (двухатомных спиртов), причем гидроксильные группы присоединяются к тем атомам, между которыми до окисления существовала двойная связь:




Алкены ненасыщенные алифатические углеводороды с одной или несколькими двойными углерод-углеродными связями. Двойная связь превращает два атома углерода в плоскую структуру с валентными углами между соседними связями по 120°С:
Гомологический ряд алкенов имеет общую формулу двумя его первыми членами являются этен (этилен) и пропен (пропилен):

Члены ряда алкенов с четырьмя или большим числом атомов углерода обнаруживают изомерию положения связей. Например, алкен с формулой имеет три изомера, два из которых являются изомерами положения связей:
Заметим, что нумерация цепи алкенов производится с того ее конца, который ближе к двойной связи. Положение двойной связи указывается меньшим из двух номеров, которые соответствуют двум атомам углерода, связанным между собой двойной связью. Третий изомер имеет разветвленную структуру:

Число изомеров какого-либо алкена возрастает с числом атомов углерода. Например, гексен имеет три изомера положения связей:
диенов является бута-1,3-диен, или просто бутадиен:
Соединения, содержащие три двойные связи, называются триенами. Соединения с несколькими двойными связями имеют общее название полиены.
Физические свойства
Алкены имеют несколько более низкие температуры плавления и кипения, чем соответствующие им алканы. Например, пентан имеет температуру кипения . Этилен, пропен и три изомера бутена при комнатной температуре и нормальном давлении находятся в газообразном состоянии. Алкены с числом атомов углерода от 5 до 15 в нормальных условиях находятся в жидком состоянии. Их летучесть, как и у алканов, возрастает при наличии разветвления в углеродной цепи. Алкены с числом атомов углерода больше 15 при нормальных условиях представляют собой твердые вещества.
Получение в лабораторных условиях
Двумя основными способами получения алкенов в лабораторных условиях являются дегидратация спиртов и дегидрогалогенирование галогеноалканов. Например, этилен можно получить дегидратацией этанола при действии избытка концентрированной серной кислоты при температуре 170 °С (см. разд. 19.2):
Этилен можно также получить из этанола, пропуская пары этанола над поверхностью нагретого оксида алюминия. Для этой цели можно использовать установку, схематически изображенную на рис. 18.3.
Второй распространенный метод получения алкенов основан на проведении дегидрогалогенирования галогеноалканов в условиях основного катализа
Механизм реакции элиминирования такого типа описан в разд. 17.3.
Реакции алкенов
Алкены обладают намного большей реакционной способностью, чем алканы. Это обусловлено способностью -электронов двойной связи притягивать электрофилы (см. разд. 17.3). Поэтому характерные реакции алкенов представляют собой главным образом реакции электрофильного присоединения по двойной связи:

Многие из этих реакций имеют ионные механизмы (см. разд. 17.3).
Гидрирование
Если какой-нибудь алкен, например этилен, смешать с водородом и пропустить эту смесь над поверхностью платинового катализатора при комнатной температуре или никелевого катализатора при температуре около 150°С, то произойдет присоединение
водорода по двойной связи алкена. При этом образуется соответствующий алкан:

Реакция этого типа представляет собой пример гетерогенного катализа. Его механизм описан в разд. 9.2 и схематически показан на рис. 9.20.
Присоединение галогенов
Хлор или бром легко присоединяются по двойной связи алкена; эта реакция протекает в неполярных растворителях, например в тетрахлорометане или гексане. Реакция протекает по ионному механизму, который включает образование карбкатиона. Двойная связь поляризует молекулу галогена, превращая ее в диполь:

Поэтому раствор брома в гексане или тетрахлорометане при встряхивании с алкеном обесцвечивается. То же самое происходит, если встряхивать алкен с бромной водой. Бромная вода представляет собой раствор брома в воде. Этот раствор содержит бромноватистую кислоту . Молекула бромноватистой кислоты присоединяется по двойной связи алкена, и в результате образуется бромозамещенный спирт. Например

Присоединение галогеноводородов
Механизм реакции этого типа описан в разд. 18.3. В качестве примера рассмотрим присоединение хлороводорода к пропену:
Отметим, что продукт этой реакции представляет собой 2-хлоропропан, а не 1-хлоро-пропан:
![]()
В таких реакциях присоединения наиболее электроотрицательный атом или наиболее электроотрицательная группа всегда присоединяются к атому углерода, связанному с
наименьшим числом атомов водорода. Эта закономерность носит название правила Марковникова.
Предпочтительное присоединение электроотрицательного атома или группы к атому углерода, связанному с наименьшим числом атомов водорода, обусловлено повышением устойчивости карбкатиона по мере возрастания числа алкильных заместителей на атоме углерода. Это повышение устойчивости в свою очередь объясняется индуктивным эффектом, возникающим в алкильных группах, так как они являются донорами электронов:

В присутствии какого-либо органического пероксида пропен реагирует с бромоводородом, образуя т. е. не по правилу Марковникова. Такой продукт называется антимарковниковским. Он образуется в результате протекания реакции по радикальному, а не ионному механизму.
Гидратация
Алкены реагируют с холодной концентрированной серной кислотой, образуя алкил-гидросульфаты. Например

Эта реакция представляет собой присоединение, поскольку в ней происходит присоединение кислоты по двойной связи. Она является обратной реакцией по отношению к дегидратации этанола с образованием этилена. Механизм этой реакции подобен механизму присоединения галогеноводородов по двойной связи. Он включает образование промежуточного карбкатиона. Если продукт этой реакции разбавить водой и осторожно нагревать, он гидролизуется, образуя этанол:
Реакция присоединения серной кислоты к алкенам подчиняется правилу Марковникова:

Реакция с подкисленным раствором перманганата калия
Фиолетовая окраска подкисленного раствора перманганата калия исчезает, если этот раствор встряхивают в смеси с каким-либо алкеном. Происходит гидроксилирование алкена (введение в него гидроксигруппы, образующейся вследствие окисления), который в результате превращается в диол. Например, при встряхивании избыточного количества этилена с подкисленным раствором происходит образование этан-1,2-диола (этиленгликоля)

Если алкен встряхивают с избыточным количеством раствора -ионов, происходит окислительное расщепление алкена, приводящее к образованию альдегидов и кетонов:
Альдегиды, образующиеся при этом, подвергаются дальнейшему окислению с образованием карбоновых кислот.
Гидроксилирование алкенов с образованием диолов может также проводиться с помощью щелочного раствора перманганата калия.
Реакция с пербензойной кислотой
Алкены реагируют с пероксикислотами (надкислотами), например с пербензойной кислотой, образуя простые циклические эфиры (эпоксисоединения). Например

При осторожном нагревании эпоксиэтана с разбавленным раствором какой-либо кислоты образуется этан-1,2-диол:

Реакции с кислородом
Как и все другие углеводороды, алкены горят и при обильном доступе воздуха образуют диоксид углерода и воду:
При ограниченном доступе воздуха горение алкенов приводит к образованию моноксида углерода и воды:
Поскольку алкены имеют более высокое относительное содержание углерода, чем соответствующие алканы, они горят с образованием более дымного пламени. Это обусловлено образованием частиц углерода:
Если смешать какой-либо алкен с кислородом и пропустить эту смесь над поверхностью серебряного катализатора, при температуре около 200 °С образуется эпоксиэтан:
Озонолиз
При пропускании газообразного озона через раствор какого-либо алкена в трихлорометане или тетрахлорометане при температуре ниже 20 °С образуется озонид соответствующего алкена (оксиран)

Озониды - неустойчивые соединения и могут быть взрывоопасными. Они подвергаются гидролизу с образованием альдегидов или кетонов. Например

В этом случае часть метаналя (формальдегида) реагирует с пероксидом водорода, образуя метановую (муравьиную) кислоту:
Полимеризация
Простейшие алкены могут полимеризоваться с образованием высокомолекулярных соединений, которые обладают той же эмпирической формулой, что и исходный алкен:
Эта реакция протекает при высоком давлении, температуре 120°С и в присутствии кислорода, который играет роль катализатора. Однако полимеризацию этилена можно проводить и при более низком давлении, если воспользоваться катализатором Циглера. Одним из наиболее распространенных катализаторов Циглера является смесь триэтилалюминия и тетрахлорида титана.
Полимеризация алкенов более подробно рассматривается в разд. 18.3.

Алкены (олефины ) – это углеводороды, в молекулах которых содержатся атомы углерода, соединенные между собой двойной связью (непредельные углеводороды ряда этилена). Простейший представитель – этилен С 2 Н 4 , общая формула гомологического ряда этиленовых углеводородов С n Н 2n (при п ≥ 2).
Систематические названия олефинов производятся от корней названий алканов с заменой суффикса – ан → – ен :
Сохраняются также традиционные названия с заменой суффикса – ан на – илен : С 2 Н 4 – этилен, С 3 Н 6 – пропилен, С 4 Н 8 – бутилен; использование названия амилен для алкена С 5 Н 10 не рекомендуется.
Положение двойной связи С=С в изомерах строения (начиная с алкена С 4) указывается цифрой после названия:
Радикал этилена – этенил СН 2 =СН – обычно называют винил, пропена – пропенил СН 2 =СН – СН 2 – именуют аллил.
Другой вид изомерии в непредельных углеводородах, помимо структурной изомерии, осуществляется потому, что атомы углерода, образующие двойную связь, находятся в sр 2 ‑гибридном состоянии; σ‑составляющая двойной связи С=С и σ‑связи С – Н лежат в одной плоскости под углом 120° друг к другу, а π‑составляющая двойной связи С=С представляет собой электронное облако, вытянутое в направлении, перпендикулярном плоскости о‑связей. Следствием такого строения алкенов является возможность геометрической изомерии (или цис‑транс‑изомерии) в зависимости от положения заместителей (атомов или радикалов):
(цис – от лат. «рядом, по одну сторону», транс – от лат. «напротив, по разные стороны»).
Алкены С 2 –С 4 при комнатной температуре – бесцветные газы со слабым запахом нефти, малорастворимые в воде; алкены С 5 –C 18 – жидкости, алкены C 19 и выше – твердые вещества.
Важнейшие химические свойства алкенов определяются тем, что в силу меньшей прочности π‑связи (по сравнению с σ‑связью) она легко разрывается, в результате чего протекают реакции присоединения и образуются насыщенные органические соединения. Как правило, такие реакции идут в мягких условиях, часто на холоду и в растворителях, например воде, тетрахлорметане СCl 4 и др.:
Аналогично протекает взаимодействие алкенов с бромоводородом:
Присоединение галогеноводородов к несимметричным алкенам теоретически может привести к двум продуктам:
Согласно правилу Марковникова, присоединение галогеноводородов к несимметричным алкенам протекает так, что водород направляется к атому углерода, который уже содержит большее число атомов водорода. В приведенной выше реакции продуктом будет 2‑иодпропан СН 3 СН(I)СН 3 .
По правилу Марковникова протекает и реакция гидратации, т. е. реакция присоединения воды в присутствии серной кислоты. Она происходит в две стадии:
а) вначале образуется алкилсерная кислота, т. е. H 2 SO 4 присоединяется к алкену:
б) затем происходит ее необратимый гидролиз:
Алкены обесцвечивают раствор перманганата калия на холоду в нейтральной среде, при этом образуются гликоли (двухатомные спирты):
Алкены способны вступать в реакции полимеризации:
Качественные реакции на алкены – обесцвечивание бромной воды и раствора КMnO 4 (уравнения реакций см. выше).
Алкадиены – непредельные углеводороды, в молекулах которых содержатся две связи С=С. Общая формула алкадиенов С n Н 2n‑2 (n ≥ 3), формула совпадает с таковой для алкинов.
Примеры :
Большое практическое значение имеют сопряженные диены, в молекулах которых связи С=С разделены одинарной связью С – С:
Дивинил и изопрен – традиционные названия.
Дивинил – бесцветный, легко сжижающийся (при ‑4,5 °C) газ, изопрен – низкокипящая (34,1 °C) жидкость.
Алкадиены вступают в те же реакции присоединения , что и алкены. Сопряженные диены имеют особые свойства, в частности, в реакциях присоединения; они образуют продукты 1,4‑присоединения с одной двойной связью посредине:
Алкадиены способны полимеризоваться с образованием каучуков:
Полиметилбутадиеновый каучук – это полимер, существующий в природе (натуральный каучук), а полибутадиеновый каучук получен искусственно (С. В. Лебедев, 1932 г.) и называется синтетическим каучуком.
Получение: для алкенов в промышленности используют метод каталитического дегидрирования алканов:
В лаборатории алкены получают:
1) дегидратацией спиртов (отщепление воды от спиртов):
2) дегидрогалогенированиеж – отщеплением галогеноводорода от моногалогенопроизводного под действием спиртового раствора щелочи:
3) дегалогенированиеж – отщеплением галогенов от дигалогенопроизводных, в которых атомы галогена находятся у соседних атомов углерода:
Промышленное получение дивинила:
1) дегидрирование бутана:
2) способ Лебедева – одновременное отщепление воды и водорода от этанола на катализаторе (ZnO/Al 2 O 3):
Алкены используются для органического синтеза, производства пластмасс, искусственного моторного топлива, диеновые углеводороды – исходное сырье в промышленном синтезе каучуков.
Алкины
Алкины – углеводороды с тройной связью C≡C в молекулах (непредельные углеводороды ряда ацетилена). Простейший представитель этого ряда – ацетилен С 2 Н 2 , общая формула алкинов C n H 2n‑2 (при n ≥ 2).
Названия простейших алкинов:
С 2 Н 2 – этин (традиционно: ацетилен)
С 3 Н 4 – пропин (метилацетилен)
С 4 Н 6 – бутин
Изомеры бутина:
Ацетилен, пропин и бутин‑1 – бесцветные газы при комнатной температуре, бутин‑2 – легкокипящая жидкость, обладает легким «эфирным» запахом.
В алкинах атомные орбитали углерода у тройной связи имеют sp‑ гибридизацию (линейное строение). Наличие двух π‑связей обусловливает их химические свойства, в частности высокую способность к реакциям ступенчатого присоединения водорода, хлора, брома, галогеноводородов, воды:
(присоединение НCl к хлорэтену происходит по правилу Марковникова; хлорэтен традиционно называют хлорвинилом или винилхлоридом);
г) реакция Кучерова (гидратация на катализаторе)
При циклизации ацетилена образуется бензол:
Упомянутый выше хлорвинил способен полимеризоваться:
Поливинилхлорид (ПВХ) – полимер, основа пластмассы, волокон и пленок, применяется в производстве труб, искусственной кожи, электроизоляции, пеноматериалов.
Качественные реакции:
1) на алкины любого строения – обесцвечивание раствора КMnO 4 , чаще всего происходит разрыв углеродной цепи по месту тройной связи (ср. с алкенами);
2) на алкины с концевой тройной связью – замещение концевого атома водорода на медь (I) с образованием ярко‑красного осадка:
Получение: в промышленности ацетилен ранее получали гидролизом дикарбида (ацетиленида) кальция:
(неприятный «карбидный» запах газа обусловлен примесями, главным образом фосфином РН 3).
Современный способ – пиролиз (термическое разложение) метана:
В лаборатории для получения ацетилена и его гомологов используют взаимодействие дигалогенопроизводных алканов со щелочами в спиртовом растворе при нагревании:
(обязательное условие – атомы галогенов должны находиться при соседних атомах углерода). Эта реакция может проходить в одну стадию (как показано выше), но чаще – в две стадии:
Алкины, особенно ацетилен, используются как исходное сырье в химической промышленности для многих органических синтезов. Кроме того, ацетилен благодаря высокой теплотворной способности сгорания:
применяется для автогенной сварки и резки металлов.
Арены
Арены – это непредельные углеводороды, которые можно рассматривать как производные простейшего из них – бензола С 6 Н 6 . Общая формула углеводородов гомологического ряда бензола С n Н 2n‑6 (при n ≥ 6).
В молекуле бензола все атомы углерода находятся в sр 2 ‑гибридизации, каждый атом углерода соединен в одной плоскости σ‑связями с двумя другими атомами углерода и одним атомом водорода. У атома углерода остается еще облако четвертого валентного электрона, расположенное перпендикулярно плоскости. Эти облака участвуют в образовании π‑связи, причем в молекуле образуются не три отдельные π‑связи (как думали раньше, см. формулу Кекуле, 1865 г.), а единая шестицентровая (С 6) π‑связь (все атомы равноценны):
Формула Кекуле часто применяется в тех случаях, когда необходимо более наглядно представить протекание реакции с участием бензольного кольца С 6 ; его изображение:
В обеих формулах атомы С кольца и не участвующие в реакции атомы Н опускаются (для краткости). Некоторые простейшие гомологи бензола:
Радикал бензола С 6 Н 5 называется фенил, радикал толуола С 6 Н 5 СН 2 – бензил.
Бензол и его ближайшие гомологи – жидкости без цвета, но с характерным запахом, имеют широкий интервал жидкого состояния. Практически не растворяются в воде, но хорошо смешиваются между собой и с другими органическими растворителями. Пар бензола сильно ядовит.
Несмотря на формальную непредельность, бензол отличается высокой устойчивостью к нагреванию и окислению (в гомологах бензола окисляется только боковая цепь). Характерными для бензола являются реакции замещения :
а) нитрование в присутствии концентрированной серной кислоты на холоду:
б) галогенирование в присутствии галогенидов железа (III):
в) алкилирование в присутствии хлорида алюминия:
Особый характер ненасыщенности бензола и его гомологов иллюстрируется этими химическими свойствами и называется «ароматическим» характером.
В производных бензола атом или группа, заместившие водород кольца, и само бензольное кольцо влияют друг на друга. По характеру влияния различают:
1) заместители I рода – CI, Br, I, СН 3 , С n Н 2n+1 , ОН и NH 2 . Они облегчают реакции дальнейшего замещения и направляют второй заместитель по отношению к себе в орто‑ (о‑, или 2‑) положение и в пара‑ (п ‑, или 4‑) положение [для запоминания: о рто – о коло, п ара – п ротив], например:
2) заместители II рода – NO 2 , С(Н)O, СООН и CN. Они затрудняют реакции дальнейшего замещения и направляют второй заместитель в мета‑ (м ‑, или 3‑) положение, например:
Очевидно, что существуют два орто‑ положения рядом с первым заместителем X, два мета ‑положения, отделенные от первого заместителя одним углеродом кольца, и лишь одно пара ‑положение через два атома углерода бензольного кольца:
Ранее уже отмечалось, что бензол стоек к окислению даже при действии сильных окислителей. Гомологи бензола с одним боковым радикалом вступают в реакции окисления только за счет радикала; при этом, какова бы ни была его длина, отщепляется вся цепь, кроме ближайшего к кольцу атома углерода (он создает карбоксильную группу):
В жестких условиях бензол вступает в реакции присоединения :
Стирол C 6 H 5 –CH=CH 2 , как этилен, легко полимеризуется:
Полистирол – термопластичная пластмасса (термопласт), прозрачный материал, размягчающийся при температуре выше 80 °C. Используется для изготовления изоляции электропроводов, посуды разового употребления, упаковочной массы (пенопласт).
Получение аренов – ароматизация алифатических и алициклических углеводородов, содержащихся в нефтяных или буроугольных бензиновых фракциях:
1) дегидрирование :
2) дегидроциклизация :
3) тримеризация ацетилена (устаревший способ):
Бензол и его гомологи используются в качестве малополярных растворителей (для каучука, лаковых смол, полимеров), сырье в органическом синтезе.